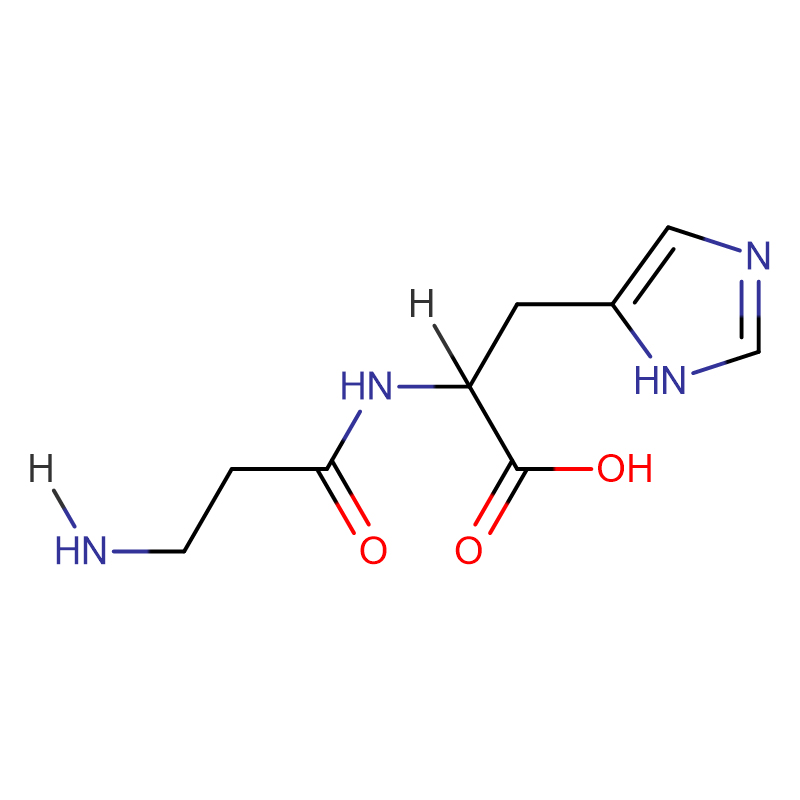
Ксантиноксидаза CAS: 9002-17-9
| Каталог нөмірі | XD90392 |
| Өнім атауы | Ксантиноксидаза |
| CAS | 9002-17-9 |
| Молекулалық формула | C18H29N5O10S2 |
| Молекулалық салмақ | 539,58 |
| Сақтау мәліметтері | 2 - 8 °C |
| Үйлестірілген тарифтік кодекс | 35079090 |
Өнімнің сипаттамасы
| Сыртқы түрі | Ақ ұнтақ |
Сигма рецепторы 1 (σR1) – эндоплазмалық ретикулум-митохондриялық мембранада молекулалық шаперон ретінде әрекет ете алатын опиоидты емес трансмембраналық ақуыз.(+)-пентазоцин [(+)-PTZ] сияқты σR1 лигандтары in vivo және in vitro көздің тор қабығын айқын нейропротекторлық қамтамасыз етеді.Жақында біз σR1 (σR1 KO) жоқ тышқандардың ретинальды фенотипін талдадық және жас тышқандарда (5-30 апта) қалыпты тордың морфологиясы мен функциясын байқадық, бірақ теріс скотопиялық шекті жауаптар (nSTRs), ретинальды ганглион жасушаларының (RGC) жоғалуы және бұзылуы төмендеді. 1 жылға ішкі торлы қабық дисфункциясына сәйкес келетін оптикалық жүйке аксондарының саны.Бұл деректер бізді σR1 созылмалы ретинальды стрессті болдырмауда маңызды болуы мүмкін гипотезаны тексеруге әкелді;қант диабеті созылмалы стресс үлгісі ретінде пайдаланылды. σR1 (+)-PTZ нейропротекторлық әсерлері үшін қажет екенін анықтау үшін жабайы типтегі (WT) және σR1 KO тышқандарынан оқшауланған бастапқы RGC ксантин-ксантин оксидазасының (10 мкМ) әсеріне ұшырады: 2 мУ/мл) (+)-PTZ бар немесе жоқ тотығу стрессін индукциялау үшін.Жасуша өлімі терминалдық дезоксинуклеотидил трансфераза dUTP nick end labeling (TUNEL) талдауымен бағаланды.Созылмалы стресстің RGC функциясына әсерін бағалау үшін стрептозотоцинді қолдану арқылы 3 апталық C57BL/6 (WT) және σR1 KO тышқандарында қант диабеті төрт топты алу үшін индукцияланды: WT диабеттік емес (WT емес ДБ), WT диабеттік (WT-DB). ), σR1 KO DB емес және σR1 KO-DB.12 апталық қант диабетінен кейін, тышқандар 15 апталық болғанда, көзішілік қысым (IOP) тіркелді, электрофизиологиялық тестілеу жүргізілді (соның ішінде nSTR анықтау) және RGC саны ретинальды гистологиялық секцияларда есептелді. In vitro зерттеулер көрсеткендей, (+)-PTZ σR1 KO тышқандарынан жиналған RGC-тердің тотығу стрессінен туындаған өлімін болдырта алмады, бірақ WT тышқандарынан жиналған RGC өлімінен сенімді қорғаныс берді.Қант диабетінен туындаған созылмалы стрессті зерттеулерде тінтуірдің төрт тобында өлшенген IOP қалыпты диапазонда болды;дегенмен, σR1 KO-DB тышқандарының IOP (16 ± 0,5 ммH г) сыналған басқа топтармен салыстырғанда (σR1 KO DB емес, WT DB емес, WT-DB: ~12 ± 0,6 mmHg) айтарлықтай артты. ).Электрофизиологиялық тестілеуге қатысты, σR1 KO DB емес тышқандардың nSTRs 15 аптада WT DB емес тышқандарға ұқсас болды;дегенмен, олар σR1 KO-DB тышқандарында (5 ± 1 мкВ) басқа топтармен салыстырғанда айтарлықтай төмен болды, соның ішінде, атап айтқанда, σR1 KO-nonDB (12±2 мкВ).Күтілгендей, σR1 KO DB емес тышқандардағы RGC саны 15 аптада WT DB емес тышқандарға ұқсас болды, бірақ қант диабетінің созылмалы күйзелісі кезінде σR1 KO-DB тышқандарының торлы қабығында RGC аз болды. Бұл бірінші есеп. (+)-PTZ нейропротекторлық әсерлері үшін σR1 қажет екенін анық көрсетеді.σR1 KO тышқандары жас жаста тордың қалыпты құрылымы мен қызметін көрсетеді;дегенмен, қант диабетінің созылмалы күйзелісіне ұшыраған кезде, σR1 KO тышқандарында сетчатка функционалдық тапшылығының үдеуі байқалады, осылайша ганглиондық жасушалардың дисфункциясы диабеттік емес σR1 KO тышқандарына қарағанда әлдеқайда ерте жаста байқалады.Деректер σR1 ретинальды стрессті реттеуде шешуші рөл атқарады және тордың аурулары үшін маңызды мақсат болуы мүмкін деген гипотезаны қолдайды.